编者按:第34届欧洲泌尿外科年会(EAU19)已于当地时间3月19日在西班牙巴塞罗落下帷幕。复旦大学附属中山医院郭剑明教授研究团队在肾癌精准医疗分会场展示了近期两项肾癌免疫研究成果,会后郭教授与《肿瘤瞭望》分享了肾癌免疫治疗进展及其团队研究。
无论国内还是国外,肾癌都是泌尿系统中发病率较高的恶性肿瘤之一。早期肾癌治疗及时,患者五年生存率为70%~80%,如果出现转移,患者五年生存会降到20%左右。对于转移型肾癌传统方法是采用TKI治疗,随着近年来免疫治疗在肿瘤领域的不断升温,纳武利尤单抗作为针对肾癌的免疫检查点抑制剂已取得良好疗效。以O药和K药为代表免疫治疗药物也不断被研发,但这些免疫治疗药物目前的治疗的效果不是太理想,所以我们团队就致力于寻找影响免疫治疗的效果的因素,或者说我们通过免疫来预判病人的愈后以及免疫治疗药物的疗效。
我们团队有两篇论文在本次大会上发表,一篇是关于免疫评分的研究,我们按照配对基因来进行个体化免疫检测,通过观察提出了个体化免疫评分,可以对患者的免疫治疗以及愈后进行分层从而有助于预后的判断。另外一篇是关于免疫蛋白的研究,我们选取PAK1蛋白,PAK1蛋白高表达对免疫环境的微环境的影响比较明显,也就会影响了患者的生存状态以及免疫反应,这对我们寻找新的靶点还是有一定的益处的。
个体化免疫相关基因标记预测透明细胞肾细胞癌患者的免疫状态和肿瘤预后(Poster No.65)
这项研究主要目的是较好地预测肾癌患者术后生存及免疫状态。我们借鉴了Heinaniemi教授在Nature Methods杂志提出的配对基因表达特征算法,建立了基于单个肿瘤样本的免疫基因表达、适用于不同mRNA检测平台的肾透明细胞癌免疫评分,能够较好地预测肾癌患者术后生存及免疫状态。
本研究回顾性分析了两个具有完整基因表达数据、临床预后信息的肾透明细胞癌队列,将纳入的101例日本肾透明细胞癌患者的SATO队列作为发现队列,534例国际癌症基因组图谱中肾透明细胞癌患者的KIRC队列作为验证队列,根据免疫相关基因相对表达高低在发现队列中构建了18万个免疫相关基因对,并从中选择153个具有区分价值、预后价值的基因对。我们进一步利用LASSO回归筛选出21个非线性相关基因对,据此建立肾透明细胞癌免疫评分,根据评分将肾癌患者分为高免疫风险组和低免疫风险组。
结果显示:在验证队列中,高免疫风险患者其总体生存、无复发生存、疾病特异性生存较低免疫风险患者均显著缩短。通过多因素回归校正肿瘤分期、分级后,免疫评分仍是肾癌患者术后生存的独立不良预后因子。免疫评分与临床病理特征结合构建的诺曼图模型预测准确性高于UISS模型,ccA/ccB分子模型。此外,免疫评分相较于目前使用最广泛的分子预后模型ccA/ccB有更好的肿瘤同质性,肾癌组织同空间位置获得的样本其检测结果较为一致。
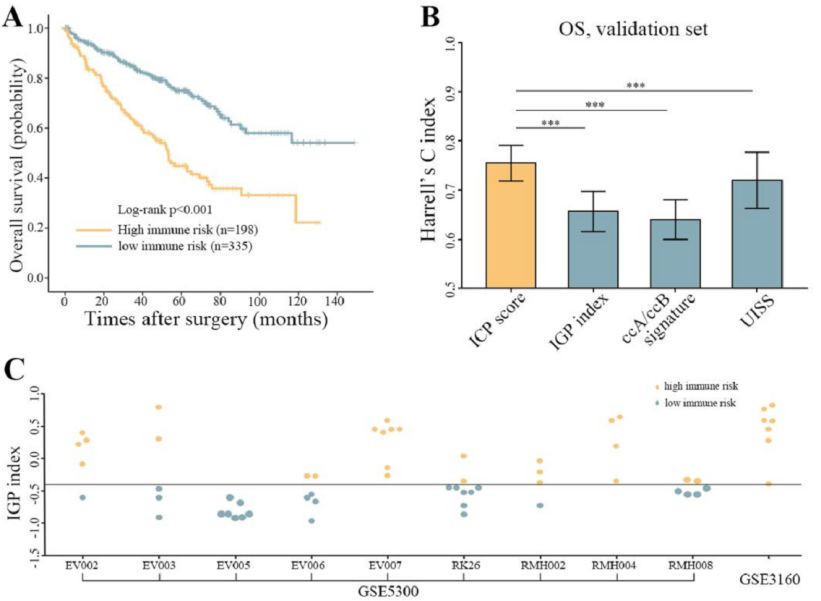
在深入分析免疫评分背后的生物学过程后发现,高免疫风险肾癌组织中有更多的免疫抑制调节性T细胞、巨噬细胞和中性粒细胞浸润,而发挥抗肿瘤免疫功能的自然杀伤性细胞浸润显著减少。免疫逃逸特征性基因复合表达水平以及适应性免疫反应负向调控通路在高免疫风险肾癌患者中显著高于低免疫风险患者,此结果提示高免疫评分肾癌患者的免疫抑制状态可能是导致其生存时间缩短的主要原因。
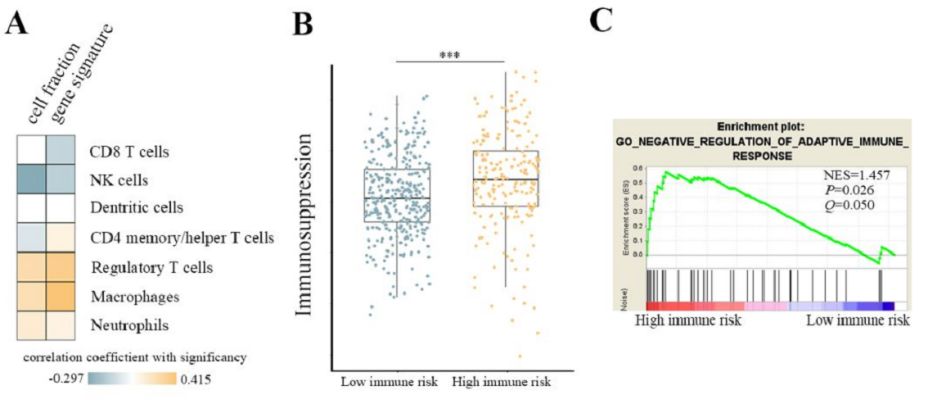
肿瘤浸润调节性T淋巴细胞与PAK1的协同作用使肾透明细胞癌产生免疫逃避(EAU19摘要号:AM19-2032)
我们对肾癌免疫治疗及其耐药机制也进行了深入研究,遴选最佳免疫治疗获益群体以指导个体化治疗。这项研究纳入了我院2005~2007年收治的282例肾透明细胞癌患者(中山医院队列),通过免疫组化检测PAK1、CCL22在肾癌组织表达情况以及Treg细胞、CD8+T细胞在肾癌组织的浸润情况,同时收集30例肾透明细胞癌患者外周血和新鲜切除肿瘤组织建立新鲜临床样本队列(FCS队列),利用流式细胞术及RT-PCR等技术检测各相关免疫细胞与PAK1、CCL22的相关性。最后利用TCGA数据库中的KIRC队列(534例肾透明细胞癌样本)进行生物信息学分析,综合评估验证该假说。
研究首先发现肾癌组织PAK1蛋白表达存在异质性,PAK1高表达提示患者的不良预后以及肿瘤组织抑制性肿瘤免疫微环境的存在。这说明PAK1促癌信号可能通过调节肿瘤免疫微环境参与肾癌进展。
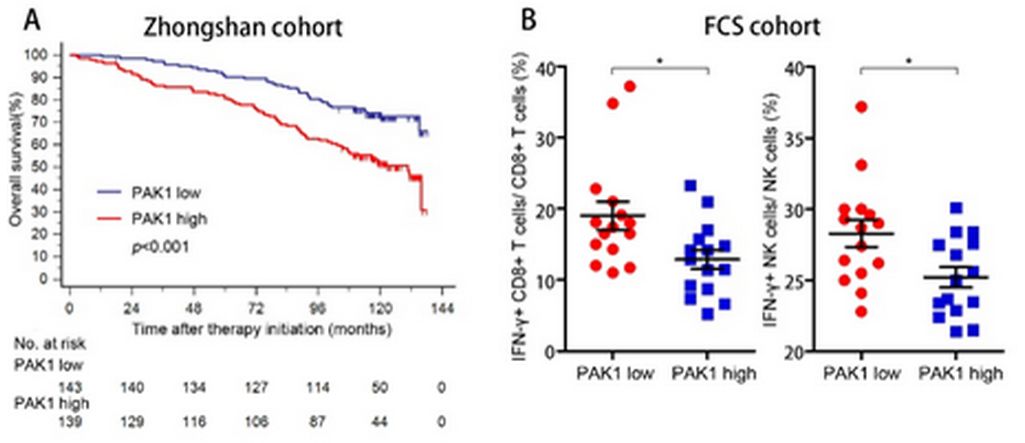
我们进一步分析发现,在多种调节性免疫细胞中,Treg细胞的浸润数量与PAK1表达最为相关,同时IL-10+Treg细胞功能表型占据主导调节地位,其与杀伤性T细胞的数量呈显著负相关。TCGA数据库的基因差异表达分析也确认了Treg细胞的免疫抑制功能。提示肿瘤浸润Treg参与了PAK1活化型肾癌的免疫逃逸过程。
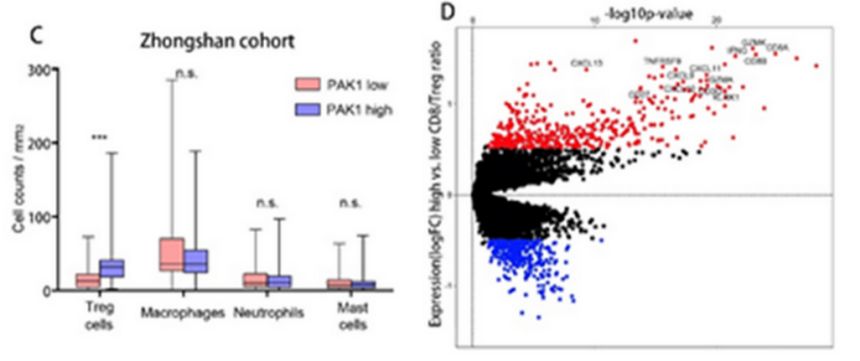
进一步探讨PAK1促进Treg细胞浸润的机制发现,趋化因子CCL22与PAK1的表达显著正相关,在加入PAK1抑制剂处理后,肿瘤组织悬液中CCL22的浓度受到显著抑制。提示PAK1可通过促进肿瘤细胞分泌CCL22,进一步招募Treg细胞向瘤内浸润,介导肾癌细胞免疫逃逸。
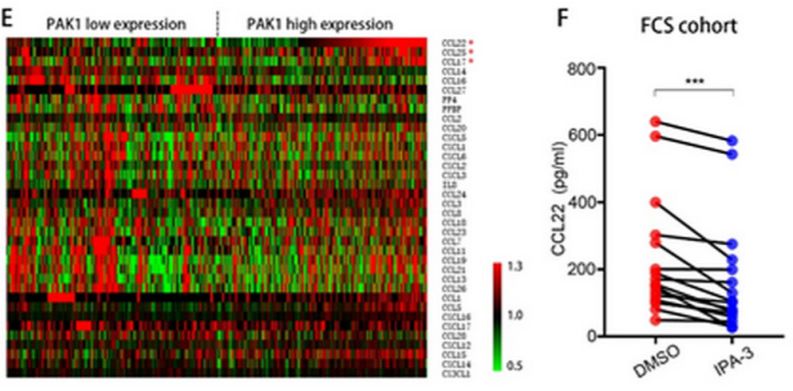
这项研究发现了肿瘤浸润Treg细胞参与调节促癌信号PAK1介导肾癌进展的功能学意义,利用临床样本的分析使得该结论贴近真实世界,对PAK1作为肾癌分子标志物及其干预的研究具有一定的临床应用价值。我们也将继续深入探讨PAK1调控肾癌免疫逃逸的分子机制,尤其是PAK1抑制剂治疗肾癌患者的转化医学价值。
专家简介
复旦大学附属中山医院泌尿外科主任,主任医师,教授,博导。从事泌尿系肿瘤临床诊疗和转化医学研究二十余年,以通讯作者身份在J Urol、BJUInt、Cancer ImmunolImmunother、J Am CollSurg等国际著名泌尿外科期刊发表SCI论文约50篇,作为分中心负责人参与泌尿系肿瘤多中心临床试验10余项。





 京公网安备 11010502033352号
京公网安备 11010502033352号